- Хімічні властивості алканів: розкриття таємниць
- Молекули прості — їх складність вражає
- Наявність простих зв’язків C-H і їх стійкість
- Цікаві хімічні пригоди алканів
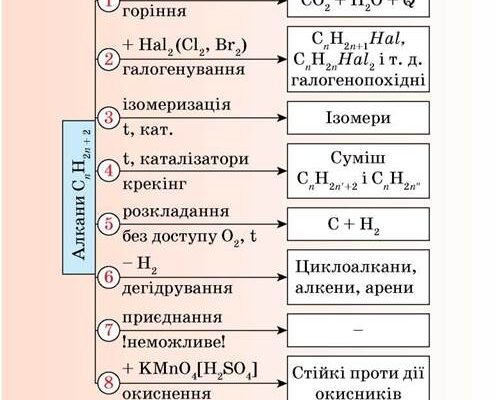
- Горіння — найпростіший спосіб отримати енергію
- Галогенування: геть нудні реакції — до більшого видовища!
- Крекінг: розбивай, щоб здобути головну суть
- Не всі загадки розгадані
- Інша сторона: ізомеризація в дію
Хімічні властивості алканів: розкриття таємниць
Алкани – ось хто тримає багатьох хіміків у постійному напруженні. Здавалося б, прості молекули, але їхні хімічні властивості можуть змусити замислитися навіть найдосвідченіші уми. Тож що робить алкани унікальними?
Молекули прості — їх складність вражає
Коли говоримо про алкани, ми маємо на увазі цілу низку молекул, насичених вуглеводнів, які мають тільки прості хімічні зв’язки (C-H). На перший погляд, нічого особливого — лише вуглець і водень, з’єднані в нескінченних ланцюгах.
Наявність простих зв’язків C-H і їх стійкість
В одній із найважливіших характеристик алканів – міцності зв’язків (C-H) і (C-C). Саме це додає молекулам неабиякої стабільності. Думаєш, що це робить їх непридатними до хімічних реакцій? О, ти помилявся б. Вони як герої екшн-фільмів: ніколи не здаються.
Цікаві хімічні пригоди алканів
Горіння — найпростіший спосіб отримати енергію
- Хімічні реакції. Коли алкани горять у повітрі, відбувається екзотермічна реакція. Разом із киснем вони утворюють вуглекислий газ і воду, віддаючи багато енергії. Дуже багато. Що цікаво— це найбільш розповсюджена використання алканів у повсякденному житті. Палаючи, вони гріють нашу оселю чи заводський котел.
- Інше. Своєю чергою, горіння може бути повним і неповним, залежно від кількості кисню. Останнє, можливо, й не таке бажане, адже утворює сажу та чадний газ.
Галогенування: геть нудні реакції — до більшого видовища!
Алкани вступають у реакції галогенування, які— так-так, ти правий— відносяться до радіаційних. Процес простий: заміна одного або більше атомів водню на галогени. Ну хіба не чудові метаморфози?
- Спільне завдання. Галогени, зокрема хлор і бром, взаємодіють з алканами за умов світла. Реакція супроводжується виділенням тепла— енергійним вибухом хімічної енергії.
- Основні реакції. Хлорування— класична реакція. Обираєш болотник з хлором, й отримаєш хлоровані вуглеводні. Вони, в свою чергу, мають багато непоганих застосувань— відповідають за різні вироби. Наприклад, полівінілхлориди у пластику.
Крекінг: розбивай, щоб здобути головну суть
Що ще цікавого можна зробити? Так, про крекінг ти вже чув. Це метод розділення великих алканових молекул на менші, легші молекули вуглеводнів. Просто – але глибоко!
- Тепловий та каталізаторний крекінг: Обидва методи мають свої нюанси. Тепловий крекінг зазвичай проводять за високих температур без каталізаторів, а його молодший брат – каталізаторний – із відповідними хімічними сполуками.
- Переваги: Багато нафтових компаній люблять його. Чому? Бо це дозволяє збільшити вихід легких фракцій, таких як бензин.
Не всі загадки розгадані
Інша сторона: ізомеризація в дію
Ізомеризація – суть простору. Перетворює лінійні алкани на розгалужені. Робить це за умов ніжної уваги кислотних каталізаторів.
- Структурна гнучкість: Дивно, але одна й та сама формула може мати іншу структуру. Звісно ж, різноманіття ізомерів дозволяє створювати нові, більш корисні хімічні речовини.
- Область застосування: Паливна промисловість сильно цінує цю реакцію. А ще вона дозволяє підвищити октанові числа бензинів.
Ну що скажеш? Алкани, незважаючи на свою міцність і стабільність, так само цікаві, як деталі трилера з безліччю сюжетних ліній. А якщо вже ти почувся героєм чи навіть вченим-уковувачем, що розкриває їх секрети, то нескінченні можливості науки відкриті до пізнання та досліджень!